首先,这种将猪的心脏移植到人身上而最初几周内没有出现急性排斥反应,就是一个巨大的进步。异种移植成功后,移植物在超声心动图上表现良好,并维持心血管和其他器官系统功能,直到术后第 47 天发生舒张性心力衰竭。术后第 50 天,心内膜心肌活检显示毛细血管受损,伴有间质水肿、红细胞外渗、罕见的血栓性微血管病和补体沉积。
报告显示:虽然研究人员使用的免疫抑制剂量虽然低于标准方案,但仍足以耗尽外周B和T淋巴细胞。然而,术后第2天提取的淋巴结显示B细胞和T细胞仍然存在。根据外周血单核细胞术分析:外周B淋巴细胞自始至终保持较低水平,并在术后第50天后重新出现。T淋巴细胞在前10天被有效耗尽,但随后又重新填充。
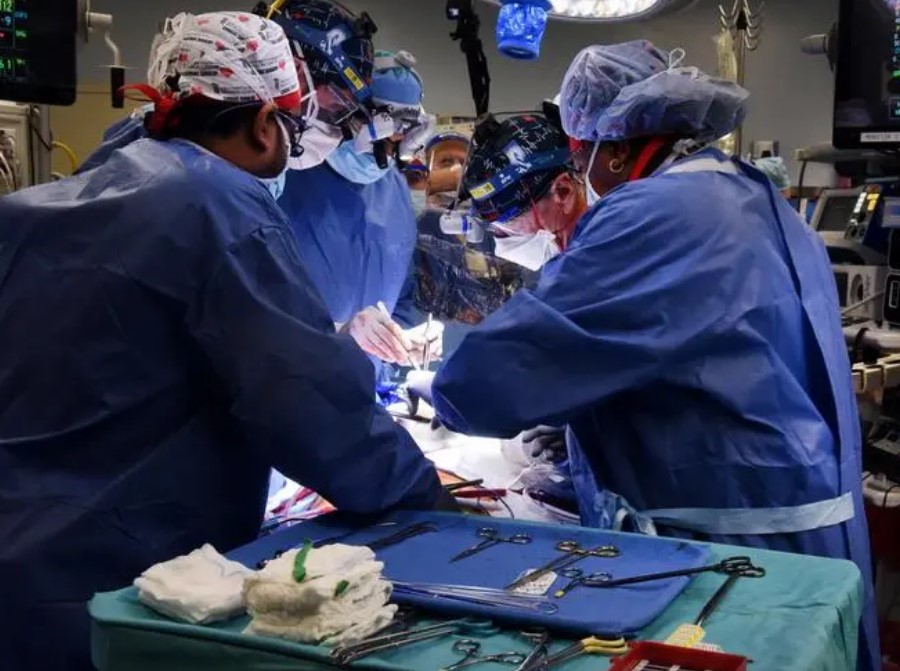
心内膜心肌活检显示:术后第34天,心肌轻度间质水肿,内皮轻微损伤,具有提示细胞凋亡的特征。术后第50天,心肌存在明显的间质水肿,并有一堆杂乱的内皮和单核细胞。术后第59天,间质内有大量细胞碎片,部分区域有红细胞外渗。报告显示:患者接受了两次高剂量IVIG(静脉注射免疫球蛋白),第47天的第二次剂量与患者病情显著恶化呈相关性。
此前,IVIG在体外被证明不与三重敲除的猪主动脉内皮细胞结合。然而,从未在十个基因敲除细胞中测试过这种结合。现在,研究人员观察到同一品牌和制造商三个不同批次的IVIG与供体猪主动脉内皮细胞的强结合。患者本身患有末期心力衰竭,生命已接近尾声,不符合传统心脏移植的资格,本次移植属于同情性使用,带有实验性质的。
如果是一个相对健康的人接受心脏移植,可能存活时间会延长。所以UMSOM 移植学杰出教授 Thomas E. 和 Alice Marie Hales称:“我们希望我们的下一位患者不仅能够通过异种移植存活更长时间,而且能够恢复正常生活并茁壮成长数月甚至数年。”患者出现了低丙种球蛋白血症,为预防感染,在移植后的第二个月,患者接受了两次IVIG注射,研究人员发现了针对猪心脏的抗体IgG。
在对受者体内各种病原体的微生物cfDNA进行测试时,观察到PCMV/PRV(PCMV,猪巨细胞病毒;PRV,猪玫瑰疹病毒)的cfDNA逐渐增加。尸检后,通过PCR对受体和异种移植物的不同部分进行了PCMV/PRV的全面评估。在所有受体器官中均检测到PCMV/PRVDNA。此前2022年6月22日,NEJM首次发布世界首例猪心移植患者研究结果,认为患者心脏尸检结果与典型的异种移植排斥不符。
而《麻省理工科技评论》在2022年5月4日报道,认为其死亡原因可能是所移植的猪心中存在病毒。患者本身身体情况较差,同时存在很多健康问题,在解决其他健康问题的时候减少了抗病毒治疗方案,PCMV可能被激活而引发破坏性炎症。不过这一点没有直接证据。这个手术患者术后存活时间较短,案例可以说失败了,但是这个手术本身还谈不上失败,筛选更适合的患者以及调整抗病毒方案,仍具有广阔的前景,在这里也要感谢David Bennett为医学做的贡献。
能不能接受动物的心脏,污染人类基因库的问题?如果异种移植成功,移植了器官的人会长期存活,他会生孩子,移植的异种器官的基因会不会编入人体,通过生育传给后代,污染人类的基因库?
点击收藏本站,随时了解时事热点、娱乐咨询、游戏攻略等更多精彩文章。













































